Почему мы доверяем медицинским исследованиям
Мы в «Купруме» говорим, что опираемся на научные исследования, но если открывать гиперссылки в статьях, оказывается, что большинство из них ведут на крупные ресурсы вроде Uptodate или Cochrane. Это не потому, что нам лень искать отдельные статьи (а мы их и ищем, и используем), а потому что так сложнее ошибиться. Каким исследованиям с большей вероятностью можно доверять, рассказываем ниже.
Пирамида доказательности
Каждый год публикуется около трех миллионов научных статей — по статье каждые десять секунд. Не все они о медицине, но заплутать и в меньшем количестве информации легко. Такое количество намекает, что подтвердить публикацией можно даже самую экстремальную точку зрения. Поэтому ученое сообщество разработало свои критерии доверия к статьям, один из которых — уровни доказательности.
Иерархию биомедицинских доказательств, то есть надежность данных, часто изображают в виде пирамиды. Внизу одиночные мнения экспертов — их много, и слепо верить им нельзя. На самом верху — систематические обзоры с обобщенными выводами. Их доля среди статей меньше, но из-за скрупулезности анализа доверия к ним больше всего. Хотя и они могут быть неидеальны. Вот как выглядит эта пирамида.
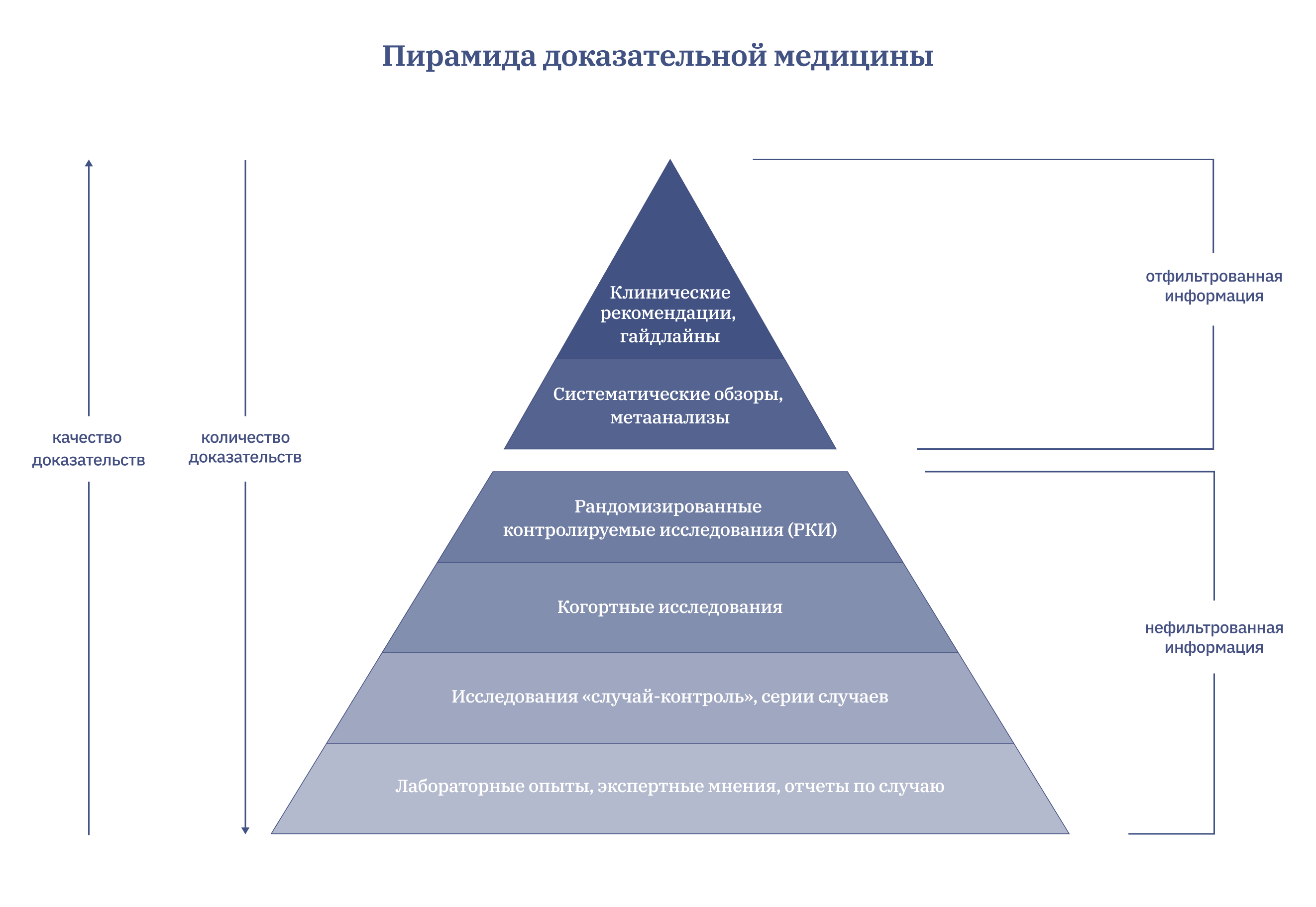
На каждом уровне есть свои эталонные методы и дизайн эксперимента. Некачественному когортному исследованию с нарушением методологии и некорректными выводами точно так же нельзя доверять, как и голословному заверению врача, что прививки вызывают аутизм.
Лабораторные опыты, экспертные мнения, отчеты по случаю
Эксперименты хороши тем, что позволяют ученым полностью их контролировать, добавлять и убирать факторы, оценивать их влияние. Единственная проблема — данные, полученные от клеток в чашках Петри или на группе мышей, нельзя распространять на людей.
Это стало очевидным не сразу — в середине 1950-х годов на рынок выпустили талидомид — успокоительное, которое не вызывало передозировки и побочных эффектов у животных. Его посчитали безопасным и для человека, но оказалось, что он вызывает врожденные дефекты плода — отсутствие конечностей, ушей, дефекты глаз и внутренних органов, с которыми родились больше десяти тысяч детей. Препарат отозвали, а отношение к регистрации лекарств пересмотрели.
Статьям об экспериментах на клетках или на животных нельзя доверять при принятии решений о здоровье. Но для мусорки они точно не годятся. Для ученых это один из этапов разработки и тестирования препаратов. Если на нем что-то пойдет не так, то дальнейших исследований с участием людей и выхода препарата на рынок просто не будет.
Такой же ненадежный источник — мнение отдельного эксперта без опоры на доказательства. Если заглянуть в новостную сводку, окажется, что один врач рекомендует от коронавируса гомеопатию, другой — от цистита пить компот, а третий скажет, что сквозняки в простудах не виноваты (и будет прав). Эксперт, даже самый уважаемый, транслирует мысли через призму своего опыта, образования, интересов и может заблуждаться.
Отчет по клиническому случаю (case report) тоже на пятом уровне в пирамиде доказательности. Он надежнее комментария, потому что отражает строгие факты.
Тщательно описанные истории болезни важны, особенно в случае редких заболеваний или неожиданных побочных эффектов. Этим методом пользовались Гиппократ и его ученики еще до нашей эры. Таким же образом на заре пандемии поступили врачи, чтобы как можно скорее рассказать о новом заболевании. Но все же по описанию одного заболевшего выводы о человечестве не сделать.
Серии случаев, исследования «случай-контроль»
Серия случаев — это отчет по нескольким пациентам с одинаковым состоянием, реакцией на препарат или лечением. Здесь исследователь, как и в одиночном отчете, не проверяет гипотезы, не ищет причинно-следственные связи или корреляции, зато тщательно фиксирует происходящее. В этой модели нет сравнения с контрольной группой, так что однозначных выводов тоже нет. Зато такие публикации вдохновляют на последующие, более продуманные исследования в области.
В исследовании типа «случай-контроль» как раз появляется контрольная группа, которая не подвергается воздействию. Две команды сравнивают по уже полученному результату, чтобы выяснить, что к нему привело. Такие исследования еще называют ретроспективными, потому диагноз уже есть, а его причину ищут в прошлом.
Например, «случай» — пациенты с сердечно-сосудистыми заболеваниями, а «контроль» — люди без них. Ученые выбирают признак, который мог бы повлиять на развитие болезни, — ежедневное употребление клетчатки, — и опрашивают о нем испытуемых. Сравнивая их ответы, исследователи ищут зависимости между группой и частотой встречаемости фактора в группе. А потом делают вывод: те, кто регулярно ест клетчатку, реже получают заболевания сердца и сосудов.
Проблема метода в том, что он обнаруживает зависимость, но не точную причинно-следственную связь. Может быть, те, кто ест много клетчатки, группа «контроль», в целом придерживаются более здоровой диеты, чем группа с сердечно-сосудистыми заболеваниями. Другое ограничение — невозможно восстановить точную последовательность событий, а оценки пациентов могут искажаться со временем. Из-за этих недостатков они посередине иерархии доказательств.
Зато исследования «случай-контроль» — это относительно быстро и недорого, особенно в сравнении с многолетними когортными исследованиями, а еще их можно применять для редких заболеваний или большого числа факторов.
Когортные исследования
Когортные исследования еще называют проспективными или лонгитюдными. Смысл один — наблюдать за выбранными группами в течение долгого времени. Например, собирают группу, которая ест много клетчатки, и группу, которая ест много переработанного мяса. Осматривают их ежегодно на протяжении 15 лет и подводят итоги — сколько людей в каждой группе получают сердечно-сосудистые заболевания. Когортные исследования могут также быть ретроспективными.
Грамотно составленные когортные исследования ценятся выше, чем «случай-контроль», потому что изменения происходят буквально на глазах у ученых. У них появляется точка старта, но каким будет результат — неизвестно. Поэтому можно наблюдать сразу за множеством маркеров и находить реальные факторы риска. В этом же и слабая сторона когортных исследований — иногда ученые не продумывают гипотезы, а смотрят сразу на все. А еще они дорогие и долгие — ну представьте сами: на протяжении нескольких лет регулярно осматривать одних и тех же людей.
Рандомизированные контролируемые исследования (РКИ)
РКИ считают золотым стандартом (но только с правильным дизайном исследования) для клинических испытаний лекарств. Рандомизация означает, что испытуемых случайно делят на две (или больше) группы. Их главное отличие: одна получает лекарство, а другая — пустышку или уже признанное лечение. Это позволяет списать любую разницу в результатах на новый препарат.
Чтобы избежать случайной подтасовки, участников дополнительно «ослепляют». Таким образом, пациенты не знают, препарат они принимают или пустышку, а при двойном слепом методе и ученые не в курсе, кого чем лечат. Так становится ясно, чем вызваны улучшения — действием препарата или верой в его эффективность.
Но не все так ладно: РКИ очень дорогие. Бывает, их спонсируют фармкомпании, из-за чего возникает конфликт интересов и подтасовка результатов. Например, в обзор плацебо-контролируемых исследований «Полиоксидония» на целую страницу вставлена реклама этого препарата.
К тому же РКИ подходят не для всего. Например, чтобы изучить действие радиации на плод, специально облучать одну группу беременных никто не будет. А для понимания, как курение влияет на детей, их не будут заставлять курить — это противоречит медицинской этике.
Систематические обзоры, метаанализы, гайдлайны
Последние две ступеньки пирамиды доказательности заняты работами, которые обобщают, перепроверяют, отфильтровывают публикации низших уровней.
В систематических обзорах рассматривают десятки статей на одну тему. Их методологию, результаты внимательно изучают, и каждый источник обретает свой вес. После чего авторы делают взвешенный вывод о пользе, эффективности, безопасности, и не на десяти испытуемых, а на сотнях или тысячах.
Метаанализ — это частный случай обзора. Разработчики заранее формулируют гипотезу, например: «Действует ли вещество N?», отбирают статьи по заданным критериям, достают числовые данные и анализируют их статистическими методами. Метаанализы позволяют сделать вывод, обобщив все цифры по конкретному вопросу. Каждый год публикуются сотни новых исследований, поэтому систематические обзоры должны регулярно обновляться.
К сожалению, известны случаи, когда заинтересованные фармкомпании спонсировали не отдельные исследования, а целые обзоры, что бросает тень на достоверность результатов. Поэтому при чтении стоит подмечать, нет ли в тексте названий конкретных препаратов и не обозначен ли в конце конфликт интересов.
Несмотря на возможные погрешности, такие исследования считаются самыми ценными с точки зрения доказательности. В их выборках тысячи и сотни тысяч человек, а значит, меньше вероятность, что эффект вызван случайностью. К тому же статьи для обзоров проверяют несколько специалистов, поэтому меньше ошибок и предвзятости.
На основе систематических обзоров создают международные клинические рекомендации. На них мы в «Купруме» смотрим в первую очередь. Эти гайдлайны отвечают на вопросы: «Как именно лечить, чтобы, скорее всего, ничего не произошло?» и «Что именно означают полученные данные?».
И что это значит
Как вы уже наверняка поняли, наука не идеальна — в исследованиях бывают ошибки, ученые могут намеренно манипулировать с их дизайном, не публиковать отрицательные результаты или подбивать под нужды фармкомпании. Но, с другой стороны, у нас появляются ответы, препараты, механизмы, инструменты борьбы с болезнями, а ученые придумывают нефальсифицируемые методы.
Мы продолжим подбирать для вас лучшие источники, а вы критически осматривайте публикуемые статьи. Иногда слово «научная» может ничего не значить.
Как вы оцениваете статью?
Комментарии (0)